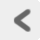3 伝導
ここまでで活動電位発生の機序、 すなわち「神経細胞膜上のある部分において 何らかの理由で閾値を超える脱分極が生じたとき膜の興奮が起こる機構」 について学習した。 しかし膜興奮は、ある地点で発生して終わり、というわけではない。 活動電位はニューロンからニューロンへと伝えられていく情報の「担い手」なのだ。 次のニューロンへとバトンを渡すため、 膜の興奮が軸索上を伝えられてこそ、はじめて活動電位の意味がある。 このようにニューロンの軸索上を活動電位が伝播することを 伝導 conductionという。
本節では、この伝導のしくみ、 すなわちある地点で発生した電位変化がどうやって伝えられていくのか を詳しく学習しよう。 (といっても答はほとんど出てしまっているのだが…。)
3.1 局所電流・局所電位
いまニューロンの軸索上の一点を、 刺激電極を用いて細胞内がプラスになるように電気刺激したとする。 その刺激による電位変化が閾値を超えると、 これまでみてきたような電位依存性イオンチャネルの開口により膜の興奮が起こる。
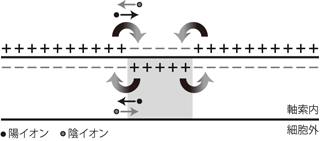
この興奮部位における電位の急上昇は、 隣接する軸索部分との間に局所電流 local currentを生じる。 すなわち、 電位依存性Na+チャネルの開口で一時的に細胞内がプラスになった部分と、 静止状態のままでマイナスの部分とのあいだで電流が生じるのだ。 この電流は軸索内ではプラスになっている興奮部位からマイナスの周囲へ、 軸索外ではプラスの周囲部位からマイナスの興奮部位へと流れる(Figure 12)。 ちなみにここでいう電流とは、 電気回路における電流のような電子の流れではなく、 荷電したイオンが溶液内を移動することで生じる電荷の移動のことである。 たとえば「細胞内で興奮部位から周囲に電流が生じる」というのは、 興奮部位で過剰になったNa+などの陽イオンが周辺領域に押し出されたり、 あるいは逆に周辺領域の陰イオンが興奮部位に引き寄せられたりするということだ。 しかし当然だが、このイオンの流れはどこまでも続くわけではない。 軸索内の長軸方向にも細胞質による抵抗が存在し、 興奮部位からより離れたところまでイオンが移動しようとすれば、 経路抵抗はそのぶん大きくなる。 そのような大きな抵抗の経路を通って移動するイオンはごく少量であり、 大部分のイオンは興奮部位から少しだけわきに移動してとまる。 すなわち軸索上のある部分の細胞内電位が一過的に上昇すると、 興奮部位からその周囲へと、近いほど多く、 遠いほど少ない量の正電荷が運ばれることになる(Figure 13上)。 その結果、興奮部位の近傍では、 興奮部位との近さに応じて正の電位変化が生じる。 この局所電流によって興奮部位周辺に生じる電位変化を 局所電位 local potentialと呼んでいる(Figure 13下)。
コラム2: イオンの移動による電流
本文中でも書いたが、 局所電流や跳躍伝導などの節で登場する細胞質基質に生じる電流は、 電子ではなくイオンの流れである。 電流とは電荷の移動に他ならないのだから、 その電荷の担い手は電子でなくても当然かまわないのだ。
しかしわたしが大学で神経科学を勉強しはじめたとき、 このことをだれも明示的にはっきりと言ってくれなかったので、 いささか悩んだ記憶がある。 もちろん金属物質に存在するような自由電子が生体の細胞内外を飛びまわっているはずがないから、 常識的に考えて、 ニューロンの電気変化云々という文脈での電流の担い手が電子ではないことは明白だ。 また高等学校でも、生物学の神経系の単元や、 化学の電解溶液の単元などで、 イオンによる電荷の移動現象はいくらでも出てくる。 しかしそれらは、あまり「電流」ということばで呼ばれないのだ。 電流といえば、多くのひとが最初に思い出すのは、 物理学で勉強した電気回路のことだろう。 この物理学において習う「電流」のイメージが強すぎると、 電子以外の媒体によって生じる電荷の移動を電流と呼んでいいのかどうか、 自信がもてなくなったりするものだ。 そのうえ大学の講義では、どの先生も「細胞内外に電流が生じて」 などとあたりまえのように言って、 誰もその実態をちゃんと明言してくれない。 こんな状態が続くと、挙句の果てには 「もしかして電解質中では電子が飛びまわれるのか?」 などという正気の沙汰ではないことを考えてしまったりする。 だから読者のみなさんがそういう混乱をしないよう、 もういちど繰り返しておく。 生理学において登場する生体内の電流とは、電子ではなく、 イオンが移動することで起こる電荷の移動のことである。
3.2 電位依存性Na+チャネルの連鎖的開口
さてもうお分かりかと思うが、 興奮部位の周囲で局所電流によって生じた電位変化(局所電位)が、 その部分の電位依存性Na+チャネルの閾値に達したらどうなるだろうか。 Na+チャネルの開口によりNa+が流入することで、 直前に興奮していた部分の周辺領域に新たな活動電位が生じるだろう。 そしてこの周囲に生じた活動電位は、そのさらに周辺部に新たな局所電位を生じる。 この繰り返しにより活動電位が軸索上で次々と生じ伝えられていくのである。 これが活動電位の伝導のしくみである。 図を用いてこれを説明しよう。
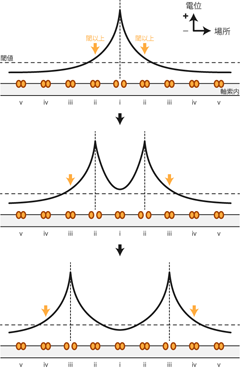
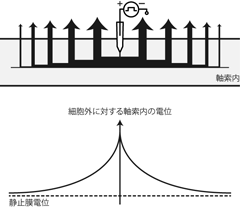
Figure 14において、 オレンジ色のたらこは電位依存性Na+チャネルを表わしている。 ただしひとつのチャネルのイラストは、 単一のチャネル分子を意味するのではなく、 膜のその部分に活動電位を引き起こすのに十分な数のチャネルの集合を表わしているとおもってほしい。 もちろん本物のニューロンにおいて、 チャネルが一定の集団で寄り集まっていたり、 同期して開閉したりするわけではない。 個々のチャネルはそれぞれ静止(活性化前)・活性・不活性(活性化後)のどれかの状態にあって、 Na+を通したり通さなかったりしているだけだ。 (チャネルの状態変化については後述する。) しかし膜上のある部分において電位を決定するのは、 その部分の近傍に存在するチャネルの総体であるため、 ここでは便宜的にそのような十分量のチャネル集団をひとつのチャネルのイラストで表現している。 また、いまは活動電位が周辺領域へと伝わっていく機序を解説しているので、 活動電位の発生に関わる電位依存性Na+チャネルのみを描いた。 もちろん軸索膜上には、 活動電位を終息させるための電位依存性K+チャネルも存在している。
さて、図においてまずiの部分で膜興奮が生じたとする。 すると、それに伴って周辺部分に山型の局所電位が生じる。 このときiの両脇のiiの部分では、 脱分極性の局所電位が電位依存性Na+チャネルの閾値を超えているので、 次の時点ではこのiiの部分で膜が興奮する。 このころにはNa+チャネルの閉鎖やK+チャネルからのK+の流出により、 iの部分の電位は静止膜電位に戻りつつある。 一方でさらに先のiiiの部分では、 局所電位が電位依存性Na+チャネルの閾値を超えたので、 次の時点で更なる膜興奮を生じる。 この繰り返しによって軸索上を興奮が伝導していく。 これこそが活動電位の伝導の機序である。
3.3 不応期
「おいちょっとまて。 なんでFigure 14の2段目で、 iiiだけでなくiの部分でも膜電位が閾値を超えてるのに、 3段目ではiiiの部分でしか興奮してないんだ?」 するどい。 これにはちゃんと理由がある。
先に電位依存性Na+チャネルの紹介をした際、 このチャネルは開口から1ミリ秒もしないうちに口を閉じると書いた。 この口を閉じた状態のチャネルは不活性状態であるといわれ、 同じ口を閉じているといっても、 開く前の「待機」の状態とは少し違う。 なぜなら待機状態の電位依存性Na+チャネルは閾値以上の電位変化に反応し開口するが、 不活性状態ではそのような電位変化に反応することができないからだ。 これはこのチャネル分子の立体構造とエネルギー遷移特性にもとづいた性質である。 不活性状態の電位依存性Na+チャネルは、 膜電位が静止レベルに戻るにしたがって徐々に待機状態へと移行し、 再び電位変化に反応できるようになる。 しかし活動電位発生直後には、 このチャネルはまだ不活性状態から待機状態へと戻っておらず、 したがって膜電位がいくら閾値を超えていてもチャネルが開口して活動電位が生じるということはない のである(Figure 15)。
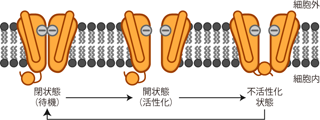
このようにいったん活動電位を発生した膜領域は、 電位依存性Na+チャネルの分子的性質により、 しばらくのあいだ再び活動電位を生じることができなくなる。 この「活動電位の直後の細胞膜が活動電位を発生できない期間」のことを 不応期 refractory periodという。
不応期には、どんなに強い入力を与えられても活動電位を発生することができない 絶対不応期 absolute refractory period (活動電位の1〜2ms後まで)と、 通常より強い刺激でなら活動電位を発しうる 相対不応期 relative refractory period(2ms後以降)がある。 絶対不応期は先に述べたとおり電位依存性Na+チャネルの不活性に因るものである。 この影響はもちろん続く相対不応期にも残っており、 相対不応期には電位変化に応答できる電位依存性Na+チャネルがまだ少ない。 しかし通常より強い脱分極刺激を与えれば相対不応期中でも活動電位を発生することから、 この状態の膜において、 必ずしも開口可能な電位依存性Na+チャネル数が絶対的に不足しているというわけではない。 どちらかというと相対不応期には、 まだ閉じていない電位依存性K+チャネルが存在するせいでK+流出が継続しており、 これを振り切って電位依存性Na+チャネルが連鎖的に開口を開始するためには、 より大きな脱分極が必要とされるものと推測される。
3.4 ニューロンの発火
前項までで、 次から次へと連続的に生じるチャネルの開閉により、 軸索上を活動電位が伝導していく過程が分かっていただけたと思う。 しかし実際のニューロンにおいては、 先ほどのモデルのように軸索の途中から活動電位がはじまることはまずない。
では伝導のきっかけとなる最初の活動電位はどこで生じるのか。 それはニューロンの細胞体と軸索の境目たる 軸索小丘 axon hillockと呼ばれる部分である。
ニューロンは、樹状突起や細胞体に他のニューロンからの情報を受け取る。 この「情報の受け取り」は、 やはり脱分極や過分極という電位変化のかたちでもたらされる。 (このプロセスは次節で扱う。) しかしじつは樹状突起や細胞体には、 ここまでみてきたような、 電位依存性Na+チャネルによって能動的に電位変化を増幅する仕組みは備わっていない。 そのため他のニューロンから与えられた電位変化は、 受け手のニューロンの樹状突起や細胞体のなかを減衰しながら受動的に拡散する。 そしてそれらの総和が、 次のニューロンへの情報の送り出しのスタート地点である軸索の付け根、 すなわち軸索小丘へと届く。
軸索小丘よりも先の軸索の膜上には、 電位依存性Na+チャネルが存在している。 だから軸索小丘の地点において、 そこに存在する電位依存性Na+チャネルを十分に活性化させられる (閾値を越える)脱分極が残っていれば、 そこで活動電位が生み出される。 生み出された活動電位は、 Figure 14でみたように、 軸索の先へ先へと電位依存性Na+チャネルの開口を誘発し、 軸索末端へと伝わっていく。 このように軸索小丘において脱分極が閾値を越えると、 軸索小丘から軸索に向けて活動電位が「発射」されるのである。 これをニューロンが発火 firingすると表現する。 よくつかう用語なので覚えておいてもらいたい。 (本項ではニューロンの活動電位発生プロセスの基本として、このような説明をした。 しかし実際には、錐体細胞の樹状突起スパイクや軸索-軸索シナプスのような機構により、 軸索小丘以外の部分から活動電位が発生することもある。)
3.5 跳躍伝導
ところでFigure 14をもう一度みてほしい。 膜上にはずらりと興奮を引き起こすためのチャネルが並んでいる。 これ、なんとなく非効率な気がしないだろうか。
たとえばヒトの脊髄を走っているニューロンには、 1つの細胞の軸索長が1mにおよぶものさえある。 この1mの軸索上にびっしりとチャネルが並び、 1回の活動電位を伝導させるたびにそれらが全部順々に活動するとしたら、 われわれはひとつの運動指令を筋肉に送るためにどれだけエネルギーを使ってしまうだろうか。 このようにチャネルの数が多すぎると、 1回の情報伝達におそろしくエネルギーがかかってしまう。 またチャネルの開閉はタンパク分子の構造変化なわけだから、 いくら1回いっかいの開閉は一瞬といっても、 バケツリレーのように隣へとなりへ回していったのでは時間がかかる。
かといって 軸索のチャネルをむやみに減らすわけにもいかない。 もしFigure 14においてチャネルの数を半分にしたらどうなるだろうか。 チャネル集団間が離れているせいで、 ある部分での膜興奮が引き起こした局所電位が、 すぐ隣の膜領域にさらなる興奮を生じさせるには不十分になってしまう。 たとえばFigure 14のiのチャネルが活性化して膜興奮が起きたとき、 iiの位置にはチャネルがなく、 一番近い隣のチャネルがiiiの位置だったらどうだろう。 この部分の膜電位は閾値に達していないから、 iiiのチャネルは開口しない。 よってiの部分で発生した局所的な興奮は周辺に伝わることなく、 減衰してしまうに違いない(Figure 16)。
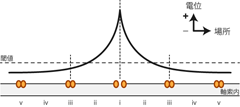
このチャネル密度では、 局所電位により隣接する膜上に生じる電位変化が閾値を超えないため、 活動電位が再生されない。
このように伝導の過程では、 うっかり活動電位が減衰して消えてしまうようなことは避けつつ、 一方で伝導にかかる時間やエネルギーは節約したい。 この悩みを一気に解決するため、 多くの生物の神経では跳躍伝導という方法がとられている。 跳躍伝導 salutatory conductionとは、 活動電位がニューロンの軸索を「跳び跳び」に伝わっていくことでエネルギーのロスを抑え、 かつ情報伝達を素早く行なうという仕組みである。 跳躍伝導にはニューロンの軸索を取り巻く髄鞘 myelin sheath という構造が関与している。 髄鞘はニューロンの軸索に巻きついてその部分を絶縁する構造である。 髄鞘によって巻かれている軸索を有髄線維 myelinated nerve fiver、 巻かれていない軸索を無髄線維 unmyelinated nerve fiverという (Figure 17)。
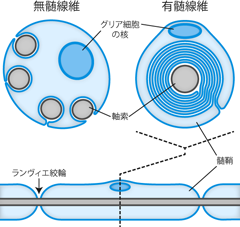
髄鞘はグリア細胞 glial cellと呼ばれる支持細胞のうち、 シュワン細胞 Schwann cellや オリゴデンドロサイト oligodendrocyte (オリゴデンドログリア oligodendroglia, 乏突起膠細胞, 希突起膠細胞, 稀突起膠細胞) という特別な細胞が、 軸索に何重にも巻きつくことによって形成される。 (シュワン細胞は末梢神経系の、オリゴデンドロサイトは中枢神経系の髄鞘を形成する。 中枢/末梢神経系などの分類は神経解剖学で扱う未学習の内容なので、 ここでは深入りしないことにする。) 髄鞘はミエリン鞘とも呼ばれ、 ミエリンという脂質の一種を特に多く含む。 このような脂質を含む細胞膜が軸索に巻きついて数十枚重なることで、 髄鞘部分における軸索膜はほぼ絶縁といえるだけの抵抗をもつ。 こうしてニューロンは軸索のまわりに絶縁性を獲得しているのである。
ただし1つの髄鞘が1ニューロンの全長にわたって軸索をおおっているわけではない。 ニューロンの軸索は一般的な細胞の大きさと比べて通常とても長いが、 1つ髄鞘の長さはおよそ1mm程度しかないのだ。 そこでニューロンの軸索全体を覆うため、 軸索上には髄鞘がいくつも連続して並んで巻きついている。 この並んでいる髄鞘と髄鞘の間には ランビエ絞輪 node of Ranvierと呼ばれる「すきま」がある。 髄鞘に巻かれている部分と違い、 ランビエ絞輪においては軸索の細胞膜が細胞外の基質と接している (Figure 2, 17)。
では軸索に髄鞘が巻きつくと、 なぜチャネルの数を節約することができるのだろう。 さきほどまで考えてきた髄鞘のない軸索(無髄線維)のモデルと比較する形で、 有髄線維における伝導のプロセスをみていこう。
先項で見たとおり、 ある部分で生じた膜興奮は隣接する電位依存性Na+チャネルを局所電位によって活性化し、 この連鎖により活動電位の伝導が起こる。 このとき局所電位は興奮している部分から離れるにつれて小さくなった。 これは正電荷を運んでいる局所電流が、 軸索内から徐々に軸索外へと流出するためである。 では軸索を髄鞘で巻くとどうなるだろうか。 髄鞘は高い絶縁性をもつため、 髄鞘が巻きついている部分では局所電流はほとんど細胞外へと流出せず、 したがって局所電流から生じる 局所電位もより遠くまで大きな値を維持できることになる。 言い換えれば、軸索を髄鞘で巻くことによって 局所電位の減衰が少なくなるのである。
さて、ここでもう一度Figure 14をみてほしい。 この図において軸索上にこれほど密にチャネルが必要なのは、 局所電位がすぐに減衰してしまうからだ。 減衰した局所電位を再生するため、 局所電位が閾値を下まわる地点よりも近傍に、 次のチャネルが存在する必要があるのだ。 逆にいえば、局所電位があまり減衰しないのなら、 これほど密なチャネルはいらない。 すなわち髄鞘によって局所電位の減衰が少なくなり、 より遠くまで電位が閾値レベルを下まわらないなら、 その間の電位依存性チャネルは節約することができる(Figure 18)。
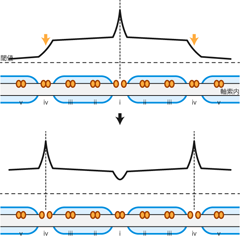
もちろん髄鞘部分の軸索においても減衰がまったくないというわけではない。 ほぼ絶縁だとはいえ、 膜興奮部位から長く離れれば局所電位はそれなりに減衰してしまう。 そこで有髄線維においても、 髄鞘と髄鞘の切れ目であるランビエ絞輪では、 無髄線維と同様ホジキンサイクルによって興奮を再生する。 このように髄鞘部分を跳び越してランビエ絞輪でのみ膜興奮が起こることが、 跳躍伝導ということばの語源になっている。
跳躍伝導は、活動電位の伝播にかかる時間も大きく短縮する。 伝導において各プロセスにかかる時間を考えよう。 伝導では軸索の一部で膜が興奮するとこれによって局所電流が流れ、 軸索上の近い部分に局所電位が生じるのだった。 この電流の流れる速さは十分に速く、局所電位は一瞬で生じる。
一方これによって閾に達した隣の電位依存性Na+チャネルが活性化し、 膜興奮を再生するプロセスでは、 チャネルタンパクの立体構造変化や膜を挟んだイオンの拡散などに比較的時間がかかる。 またこれらのプロセスのあとには、 細胞内外のイオン濃度勾配を再生するため Na+-K+ポンプによる能動輸送を行わなければならず、 エネルギーも消費してしまう。 つまり伝導において時間と労力を要するのは、 チャネルを開閉して活動電位を再生するこのプロセスである。 そして有髄線維では局所電位の減衰を少なくすることで、 必要とされる活動電位再生のプロセスの回数を減らし、 それによって伝導の時間短縮とエネルギー節約を成し遂げているのである。 実験により得られた有髄・無髄線維の伝導速度を比べれば、 跳躍伝導の効果の高さが明らかになる(Table 3)。
| 形態 | 機能 | 伝導速度 |
|---|---|---|
| 体位置の感覚線維 | 70–120 [m/s] | |
| 有髄線維 | 触覚・圧覚線維 | 30–70 [m/s] |
| 痛覚・温覚線維 | 12–30 [m/s] | |
| 無髄線維 | 交感神経節後線維 | 0.7–2.3 [m/s] |
髄鞘化は脳の進化的な複雑化にも貢献している。 いまみてきたように、 髄鞘によって軸索をおおい有髄線維にすることで、 活動電位の伝導速度をあげることができる。 そして当然ながら、 神経信号をより速く伝えることは、 個体の生存に直結する。 それでは、もし髄鞘なしで伝導速度をあげようとしたら、 どうすればよいだろう。 ニューロンの軸索を一種の電気ケーブルと考えると、 髄鞘のような特殊な構造なしに信号の伝播速度をあげるには、 ケーブルの断面積を大きくすればよい。 これは高等学校で習う物理学の基本だ。 実際ヤリイカの巨大軸索のように、 ヒトと異なる進化をした生物群のなかには、 この方略を用いているものもいる。 しかしニューロンにおいて軸索径を太くすることは、 ひとつの細胞が大きなスペースを占有し、 またその細胞の維持によりたくさんのエネルギーを必要とすることを意味する。 つまり伝導速度の向上のために軸索を太くしようとすると、 神経系全体が保持できるニューロン数が、 スペース的にもエネルギー的にも制限されてしまうのだ。 よってそのような進化方略をとった生物の神経系は、 必然的に構成細胞数の少ない比較的単純なネットワークしか実現しえない。
しかし軸索を髄鞘で巻いて絶縁性を高めれば、このような無駄を回避し、 ニューロン数を犠牲にすることなく伝導速度を向上することができる。 すなわち髄鞘は、 活動電位の伝導において時間的・エネルギー的節約を可能にするのみならず、 多数のニューロンで複雑な神経回路を組むためのスペースの確保にも一役買っているのである。 このように考えると、 われわれヒトが非常に複雑な脳の神経ネットワークを進化させることができたのも、 髄鞘化という戦略のおかげということもできるだろう。
このように有髄線維と無髄線維の伝導速度の違いはじつに顕著である。 軸索を絶縁体で巻くという単純な工夫が、 生体内でたいへん大きな効果をもたらしていることが分かったとおもう。 ちなみに気になる人のために述べておくと、 Table 3において有髄線維のなかにも伝導速度にかなりの違いがあるのは、 軸索の太さや細胞内外のイオン濃度差の違いによるものである。
3.6 活動電位の意義
これまで学習してきた活動電位の伝導機構は、 生体にとってどのような意味をもっているのだろうか。
あるひとつのニューロンから見れば、 伝導はその細胞のなかを情報が運ばれていく過程である。 ここで重要なのは、ニューロンの形態が一般的な細胞とまったく異なり、 軸索という長い「ケーブル」状の構造を有しているということだ。 このケーブルをつたって情報は非常に離れた他の神経細胞へと伝えられる。 このとき軸索を伝えられる情報は、活動電位の有/無というデジタルな電気情報である。 活動電位は細胞膜上のチャネルによって再生されながら運ばれるため、 どんな長い距離も減衰せずに伝わる。 ここがポイントだ。 すなわち伝導とは、離れた場所へと情報の質を低下させずに伝える方法なのである。
先にも触れたとおり、ヒトの身体においては、 大脳皮質から下半身の筋まで「運動指令」を運ぶための1m近い軸索を持つニューロンさえ存在する。 もしこの間を、 ごく普通の小さくて丸い細胞がつながって繋いだら、 この経路だけでいったいどれだけの細胞が必要になるだろうか。 ニューロンの軸索は情報を伝える距離を稼ぐための効率的な手段なのである。 しかしこのとき、 ケーブルが長いせいで信号が途中で減衰してしまったのでは元も子もない。 たとえば素足でガラス片を踏んでしまったとき、 痛みの受容細胞が発した情報が神経を伝えられるうちに減衰して弱まり、 その結果脳が「これだけしか活動電位が来てないから、 まあ小石でも踏んだんだろう」とでも感じてしまったら困ってしまう。 このようなことにならないために、 生体内の長距離ケーブルであるニューロンの軸索には、 種々の膜タンパクによる興奮の再生・伝播機構が備わっているのである。
このように活動電位の伝導は、 長い距離を情報の劣化なく伝えるためのしくみだといえる。 これによってわれわれは、 全身と脳とのあいだで瞬時にそして間違いなく情報の連絡を行なうことができる。 この機能の達成のため、 元来アナログである生命が1/0というデジタルなシステムを進化させたことは本当に感嘆するばかりだ。 高等学校の生物などで活動電位の伝導プロセスを学習した人にとって、 本節の内容は「あたりまえ」の事項だったかもしれない。 しかしこうして改めて振り返ってみると、 その「あたりまえ」と思っている機構は、 生命が長い進化の歴史のなかで発明した精巧かつ合理的なシステムなのである。





 @kanri_ninjin
@kanri_ninjin



 イクナイ! 581
イクナイ! 581